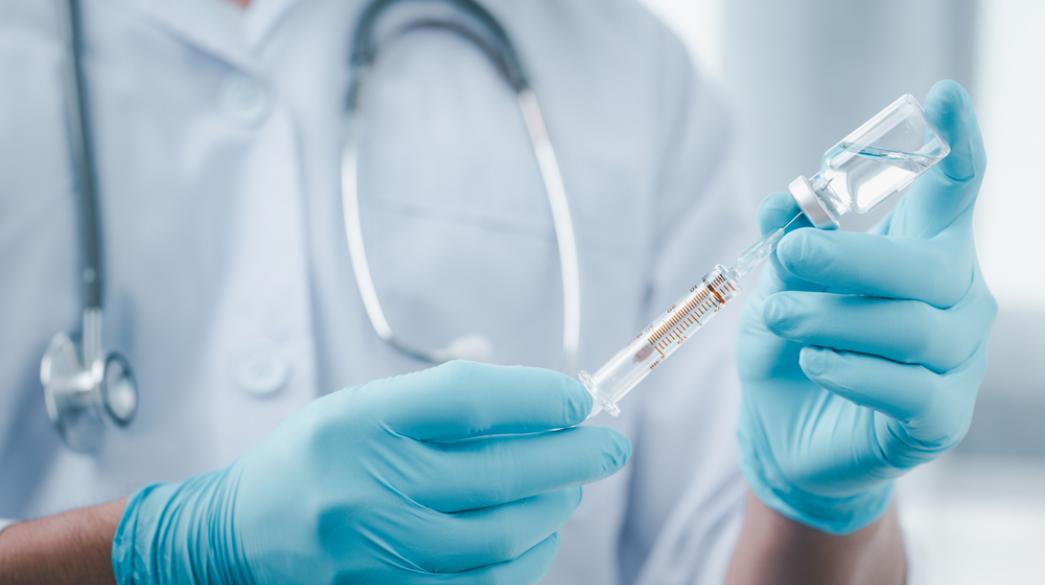
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων (ΕΜΑ) ανακοίνωσε σήμερα ότι ξεκίνησε να αξιολογεί την αίτηση της Janssen για τη χορήγηση αναμνηστικής δόσης του εμβολίου της κατά της COVID-19, τουλάχιστον δύο μήνες μετά την πρώτη δόση σε άτομα ηλικίας 18 ετών και άνω.
Η επιτροπή ανθρώπινων φαρμάκων (CHMP) του EMA θα πραγματοποιήσει μια ταχεία αξιολόγηση των δεδομένων που υποβάλλονται από την εταιρεία που εμπορεύεται το εμβόλιο. Αυτά τα δεδομένα περιλαμβάνουν αποτελέσματα από περισσότερους από 14.000 ενήλικες που έλαβαν δεύτερη δόση εμβολίου COVID-19 Janssen ή εικονικό φάρμακο (εικονική θεραπεία) δύο μήνες μετά την αρχική δόση.
Το αποτέλεσμα αυτής της αξιολόγησης αναμένεται εντός εβδομάδων, εκτός εάν απαιτηθούν συμπληρωματικές πληροφορίες, σημειώνει ο EMA.
Το εμβόλιο κατά της COVID-19 της Janssen, επί του παρόντος, έχει εγκριθεί για χρήση σε άτομα ηλικίας 18 ετών και άνω, με τον αρχικό εμβολιασμό να αποτελείται από μία δόση. Το εμβόλιο αποτελείται από έναν άλλο ιό (της οικογένειας των αδενοϊών) που έχει τροποποιηθεί ώστε να περιέχει το γονίδιο για την παραγωγή μιας πρωτεΐνης από τον SARS-CoV-2, τον ιό που προκαλεί την COVID-19. Το εμβόλιο της Janssen κατά της COVID-19 δεν περιέχει τον ίδιο τον ιό και δεν μπορεί να προκαλέσει COVID-19. Το εμβόλιο λειτουργεί προετοιμάζοντας τον οργανισμό να αμυνθεί ενάντια στον SARS-CoV-2.
Ο ΕΜΑ σημειώνει ότι η υλοποίηση εκστρατειών εμβολιασμού στην ΕΕ, συμπεριλαμβανομένης της χρήσης αναμνηστικών δόσεων, παραμένει προνόμιο των εθνικών τεχνικών συμβουλευτικών ομάδων εμβολιασμού (NITAGs) που καθοδηγούν τις εκστρατείες εμβολιασμού σε κάθε κράτος-μέλος της ΕΕ. Αυτοί οι φορείς είναι σε καλύτερη θέση να λαμβάνουν υπόψη τις τοπικές συνθήκες, συμπεριλαμβανομένης της εξάπλωσης του ιού (ειδικά τυχόν παραλλαγών που προκαλούν ανησυχία), της διαθεσιμότητας εμβολίων και των δυνατοτήτων των εθνικών συστημάτων υγείας.